테고사이언스, 피부세포치료제 임상조건 충족
|
테고사이언스(대표 전세화)는 11월30일 식품의약품안전청으로부터 자기유래 피부세포치료제인 홀로덤이 국내에서 판매허가 받은 자기유래 세포치료제 중 최초로 시판 후 임상실시 허가 조건을 충족시켰다고 발표했다. 국내 세포치료제는 9사 10개 제품으로, 테고사이언스의 동종유래 피부세포치료제인 칼로덤을 제외하고 9개가 시판 후 임상실시를 조건으로 품목허가를 받았다. 홀로덤이 식품의약품안전청으로부터 허가조건을 충족함으로써 홀로덤이 안전성과 유효성이 입증된 국내 최초의 자기유래 세포치료제의 위치를 차지하게 됐다.
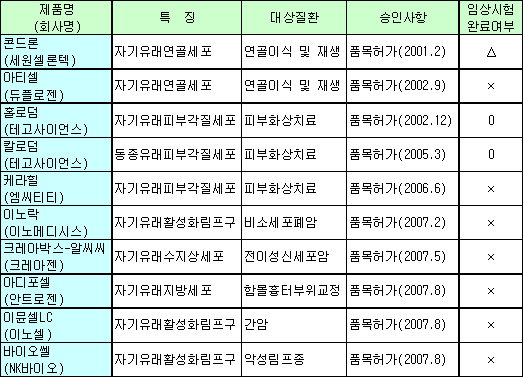
테고사이언스는 “임상시험을 실시함과 동시에 한강성심병원, 부산하나병원, 베스티안병원 등 화상전문병원을 중심으로 300여건의 임상사례를 확보하고 홀로덤의 효과를 재차 확인했다”고 밝혔다. 테고사이언스는 2001년 3월에 설립된 세포치료제 전문기업으로서 홀로덤 뿐만 아니라 2005년 3월 판매허가를 받은 동종유래 피부세포치료제인 칼로덤을 판매하고 있으며, 홀로덤이 시판 후 임상시험을 완료함으로써 국내 세포치료제의 선두주자를 달리게 됐다. 표, 그래프: | 국내 세포치료제 허가현황 | <화학저널 2007/12/18> |
||||||||||||||||