CMO(Contract Manufacturing Organization) 사업을 활성화할 필요성이 제기되고 있다.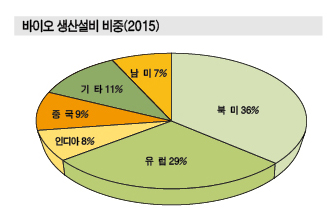
CMO 사업은 제약기업들이 위탁생산을 중심으로 성장했으며 바이오시밀러를 중심으로 바이오의약품 시장이 성장함에 따라 바이오의약 CMO에서 높은 수익이 기대되고 있다.
국내 바이오의약 CMO는 삼성바이오로직스, 셀트리온, 바이넥스 등이 생산설비를 보유하고 있으며 한화케미칼은 오송에 CMO 공장을 건설했으나 바이오사업을 정리하면서 2015년 7월 바이넥스에게 매각했다.
CMO 시장 확대로 삼성그룹은 삼성바이오에피스와 삼성바이오로직스를 설립해 바이오시밀러 개발과 생산을 함께 운영하면서 바이오사업에 사활을 걸고 있다.
삼성그룹은 수익성이 낮아질 것으로 예상되는 화학사업을 매각하고 신규사업으로 바이오의약품 사업에 집중하고 있다.
제약기업, GMP 인증 까다로워 CMO “의존”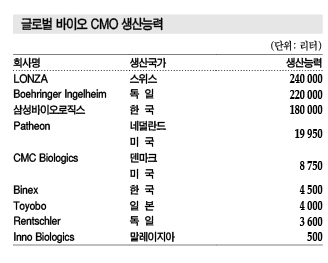
CMO는 의약품 및 원료물질 생산을 대행해 제약기업이 생산설비 건설에 비용과 시간을 투자하지 않고 신약을 확보할 수 있어 주목받고 있다.
건강기능식품 원료, 기초원료 등도 소규모로 위탁생산이 가능하며 최근에는 바이오의약품을 중심으로 가파른 성장세를 이어가고 있다.
국내에서는 셀트리온에 이어 정부가 의약품 위탁생산기관인 생물산업기술실용화센터(KBCC)를 설립해 CMO를 운영하기 시작했으며 2009년부터 10년간 바이넥스가 민간위탁 사업으로 운영을 계속하고 있다.
바이넥스는 바이오의약품 뿐만 아니라 임상시험에 필요한 신약샘플을 위탁 생산하고, 바이오신약도 생산하고 있다.
CMO는 GMP 인증이 필수적인 것으로 나타나 식품의약품안전처에서 엄격히 관리하고 있다.
국내에서 생산하는 의약품을 미국, 유럽 등 선진국에 수출하기 위해서는 미국 cGMP, 유럽 EU-GMP 등의 인증을 받아야 한다.
미국 FDA(식품의약국)는 「우수 의약품 제조 및 품질관리기준(cGMP: Current Good Manufacturing Practice)」에 부합하는 위탁 생산설비를 CMO로 승인하고 있으며 세계적으로 cGMP가 인증기준으로 혼용되고 있다.
하지만, cGMP, EU-GMP 등은 인증절차가 까다롭고 설비투자 부담이 커 제약기업들은 인증을 획득한 CMO에 의존도가 높아지고 있다.
합성의약품, 중국·인디아가 저가공세로 “장악”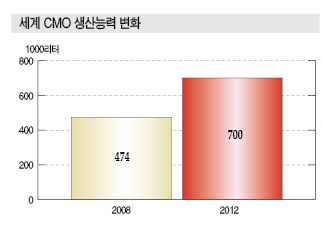
합성의약품은 대부분의 제약기업이 BGMP(Bulk Good Manufacturing Practices: 우수원료의약품 제조관리기준) 인증을 획득한 CMO에 위탁하고 있다.
국내 합성의약품 생산은 KGMP(Korea GMP)로 검증하고 있으며 BGMP 인증기업이 100여개에 달하는 것으로 나타나고 있다.
건강기능식품 등도 GMP 인증을 받으나 의약품에 비해 까다롭지 않아 국내에 100여개 생산기업이 운영되고 있다.
하지만, 국내 합성의약품 CMO는 중국, 인디아의 저가공세에 밀려 경쟁력이 떨어지고 있다.
시장 관계자는 “합성의약품 CMO 사업은 미국, 유럽 등 선진국을 중심으로 발전했으나 생산비가 저렴한 아시아의 입지가 점차 강화되고 있어 인디아·중국이 주목받고 있다”고 밝혔다.
인디아 Cipla는 선진국의 cGMP 수준으로 대규모 생산설비를 보유하고 미국 FDA와 유럽 EMEA(European Medicines Agency) 품질관리를 준수하면서 합성의약품을 위탁생산하고 있다.
다만, 바이오 CMO는 대량배양을 통한 생산비용 절감이 필수이어서 진입장벽이 높은 것으로 나타나고 있다.
또 cGMP 인증을 받아야 생산이 가능하고 엄격한 품질관리(QC: Quality Control) 단계를 통과해야 판매가 가능한 것으로 알려졌다.
삼성그룹은 약 1조원을 투입해 CMO 설비를 구축함으로써 중소기업 및 일반기업이 진입하기에는 비용 부담이 큰 것으로 판단되고 있다.
메이저, 바이오의약 CMO에 적극 투자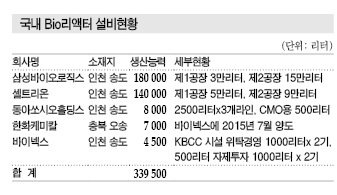
CMO는 임상용 샘플 생산에서 공정개발 지원, 임상 및 완제의약품 생산에 이르기까지 전문적인 서비스를 제공하고 있어 제약기업들의 신약 개발비용 부담을 덜어주고 있다.
특히, 바이오시밀러는 오리지널제품과 동등성을 유지하기 위해 고도의 기술력과 대규모 설비가 필요한 것으로 나타나고 있다.
특허가 만료된 의약품을 바이오시밀러로 생산함에 따라 바이오시밀러 위탁생산이 늘어나고 있어 CMO 시장도 합성의약품 생산에서 바이오시밀러 생산으로 전환되고 있다.
바이오시밀러는 생산기술 및 설비의 Validation까지 수년간 막대한 설비투자가 선행돼야 하는 것으로 나타나고 있다.
바이오시밀러 등 단백질의약품 CMO는 호르몬, 항체, 백신, 생체 기능성 단백질을 미생물·동물숙주세포에서 대량 생산해 추출하고 있어 첨단 생명공학기술이 요구되고 있다.
Boehringer Ingelheim은 1997년 미국에서 가장 오래된 위탁생산기업 Ben Venue Laboratories를 인수해 CMO 사업에 진입했고 바이오리액터(Bio-reactor) 등 생산설비를 확충해 동물세포 기반의 바이오의약품 생산능력을 세계 3위로 끌어올렸다.
Roche도 프랑스 공장을 독립 자회사로 분리해 2004년부터 CMO 사업에 진출했다.
스위스 Lonza는 1980년대부터 바이오의약품 사업에 진입해 CMO 사업을 본격화했으며 영국, 미국 등의 바이오의약품 생산설비를 인수해 규모를 확장하고 있다.
국내시장은 식약처가 2017년 세계 7대 바이오의약품 강국으로 도약하기 위해 「글로벌 바이오의약품 지원방안」을 마련했으며 CRO(수탁전문기업) 및 CMO 등 5개 분야의 경쟁력을 강화할 계획이다.
특히, 바이오의약품 CMO는 2017년 2개사를 육성할 예정이다.
중국·인디아 추격하기 이전에 선점해야…
바이오 CMO는 화학합성 의약품과 달리 생물 배양으로 생산돼 분자가 복잡하고 크기가 커 공정관리가 더 까다로운 것으로 나타나고 있다.
특히, 바이오시밀러는 생명체를 배양, 분리, 정제하는 과정에 따라 미세한 차이가 있어 동일공정을 거쳐도 단백질의 구조변형으로 오리지널과 동일제품을 만드는 것이 불가능한 것으로 알려졌다.
바이오시밀러는 개발관련 시간과 비용이 오리지널 의약품의 절반 수준에 불과하지만 승인 성공률이 80%에 육박해 신규진입이 계속되고 있다.
바이오 CMO는 바이오의약 사업 진출에 선행적으로 투자할 필요성도 제기되고 있다.
높은 영업이익률로 수익 개선이 가능하고 위탁생산으로 바이오의약 생산에 대한 경험을 축적할 수 있기 때문이다.
그러나 바이오 CMO 투자는 건설에만 3-4년이 필요하고 최소 1억-1억5000달러가 들어가 제약기업들이나 바이오의약기업의 진입이 어려운 것으로 나타나고 있다.
하지만 제약기업들이 생산을 이원화함으로써 공급안정 효과를 기대하고 있어 바이오 CMO 수요가 계속 증가할 것으로 예상되고 있다.
바이오플랜에 따르면, 바이오의약품을 자가생산하겠다는 바이오기업은 동물세포 기반 기준 2006년 57.6%에서 2013년 46.2%로 감소했고, 미생물 기반도 2006년 58.1%에서 2013년 34.8%까지 크게 들어 바이오 CMO의 의존도가 높아질 것이 불가피해지고 있다.
시장 관계자는 “바이오의약품 생산기업들은 중소기업으로 R&D에는 강하나 자금부족으로 직접 생산이 어려운 곳이 태반”이라며 “대규모 자본을 보유한 대기업들이 CMO에 집중한다면 고수익을 누릴 수 있다”고 주장했다.
다만, CMO 사업은 품질에 문제가 발생하면 제약기업들이 위탁생산 계약을 해지하는 것으로 나타나 고품질을 유지할 수 있는 기술력이 요구되고 있다.
범용 CMO를 장악하고 있는 중국, 인디아도 바이오 CMO에게 관심을 표명하고 있어 초기투자를 가속화해야 경쟁 우위를 점할 수 있을 것으로 예상되고 있다.
국내시장, 삼성그룹만 적극 투자
삼성은 삼성바이오로직스를 설립해 CMO 사업에 투자함으로써 바이오의약품 CMO에서 글로벌 경쟁력을 강화할 방침이다.
삼성바이오로직스는 3500억원을 투자한 바이오리액터 3만리터 1공장과 7000억원을 투자한 15만리터 2공장을 가동함에 따라 전체적으로 바이오리액터 18만리터 가동이 가능한 것으로 나타나고 있다.
제1공장은 FDA/EMA 실사 완료를 목표로 북미 및 유럽에 바이오의약품을 공급할 수 있도록 총력을 기울이고 있다.
바이오리액터 생산규모는 Lonza 24만리터, Boehiringer Ingelheim 22만리터로 삼성바이오로직스는 글로벌 3대 바이오의약품 CMO에 포함되고 있다.
Lonza는 CMO 전문기업으로 생산대행에 집중하고 있으며 독일 Boehringer Ingelheim은 제약기업과 CMO를 병행하고 있다.
삼성바이오로직스는 2020년까지 제3공장 15만리터, 제4공장 15만리터를 추가 증설할 가능성이 있어 글로벌 최대 바이오의약품 CMO로 등극할 가능성도 제기되고 있다.
삼성바이오로직스는 2020년 매출 1조원에 영업이익률 30-40% 수준을 기대하고 있다.
2013년 BMS(Bristol-Myers Squibb), Roche와 CMO 장기계약을 체결했고 BMS의 흑색종 치료제 「Yervoy」를 10년간 CMO 계약을 체결해 생산하고 있다.
바이오리액터는 바이넥스와 삼성 외에는 전무해 적극 투자가 요구되고 있다.
다만, 기술력과 설비투자에 수천억원이 투입됨에 따라 진입장벽이 높아 함부로 덤벼들지 못하고 있다.
한화케미칼은 오송공장에 CMO 7000리터 공장을 완공했으나 바이오의약 사업을 접고 바이넥스에게 매각했다.
셀트리온도 일부 바이오의약품 CMO를 운영했으나 자체적으로 바이오시밀러를 개발함에 따라 CMO를 운영하지 않고 있다.
셀트리온은 2002년부터 에이즈백신을 생산하기 위해 바이오리액터를 구축했으나 임상3상에서 실패함에 따라 가동이 어려웠던 것으로 알려졌다.
하지만, 2005년 BMS 및 Orencia와 장기 CMO 계약을 체결해 바이오리액터를 가동하기 시작했으며 2007년 제1공장 cGMP 승인을 받았고 2009년 BMS와의 CMO 계약이 종료됨에 따라 바이오시밀러 개발을 추진하고 있다.
1공장만 cGMP 인증을 받아 1공장에서 「램시마」를 생산하고 있으며 2공장에서는 「허쥬마」와 「CT-P10」의 임상용 샘플을 생산하고 있다.
1공장은 1만2500리터 라인이 4개, 2공장은 1만5000리터 라인이 6개로 총 14만리터를 구축하고 있으며 자가제품 생산으로 CMO 사업은 하지 않고 있고 9만리터의 3공장은 투자를 계획하고 있다.
「램시마」는 캐나다에서 바이오시밀러 최초로 판매허가를 획득했으며 미국시장에 진출하기 위해 허가신청을 완료한 것으로 나타나 cGMP 인증이 완료된 제1공장에서 생산하고 있다. <허웅 기자: hw@chemlocus.com>


























