일본 아지노모토(Ajinomoto)가 긴 사슬 리보핵산(RNA) 위탁개발‧생산(CDMO) 진출을 추진한다.
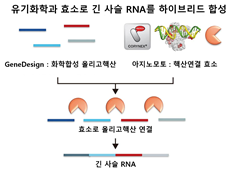
아지노모토는 핵산 CDMO 사업을 담당하는 자회사 GeneDesign과 염기가 수백개에 달하는 RNA를 제조하는 새로운 합성기술을 개발했다.
GeneDesing이 임의의 위치에 염기를 삽입한 염기 수십개의 짧은 올리고핵산을 만들고 아지노모토가 고활성 핵산 연결 효소로 연결해 긴 사슬 RNA를 제조하는 방식이다.
90% 이상의 순도를 유지하면서 짧은 사슬을 화학수식한 다음 긴 사슬로 연결하기 때문에 간단하게 의약품 활성을 개선할 수 있는 점이 특징이다.
핵산의약품은 염기가 수십개 수준인 안티센스(Antisense) 핵산과 짧은 간섭 RNA(siRNA)가 상용화되는 가운데 최근에는 코로나 백신에 사용했던 메신저 RNA(mRNA)를 비롯한 긴 사슬 RNA도 주목받고 있다.
 유전자 편집에 이용하는 가이드 RNA도 100-200개의 염기가 필요하며 화학수식한 염기를 도입하면 안정성과 활성 향상 개발이 가속화될 것으로 예상된다.
유전자 편집에 이용하는 가이드 RNA도 100-200개의 염기가 필요하며 화학수식한 염기를 도입하면 안정성과 활성 향상 개발이 가속화될 것으로 예상된다.
다만, 기존 고상합성 방식으로는 긴 사슬 RNA를 고순도로 대량 생산하기 어렵고 mRNA 생산 방식인 효소로 모노머 염기를 연결하는 전사합성은 임의의 위치에 화학수식이 불가능하다.
아지노모토가 개발한 기술은 100 염기 RNA 합성에서 고상합성의 3배를 능가하는 수율을 달성했다.
일반적인 핵산합성 수율은 이론상 98%이며 염기를 1개씩 연장할 때마다 2% 낮아지는데 고상합성은 100 염기 수율이 14% 수준으로 떨어지기 때문에 목적물을 얻기 위해서 90%에 가까운 불순물을 AN(Acrylonitrile)과 같은 용제로 정제해야 한다.
반면, 하이브리드 합성은 25 염기의 수율이 약 62%인 짧은 사슬을 연결하기 때문에 전체 수율이 45%를 유지할 수 있을 것으로 기대된다.
아지노모토는 28 염기 RNA 단편을 연결한 560 염기 mRNA 합성에 성공함에 따라 산업용 수준 대응준비가 완료된 것으로 판단하고 사업화에 나섰다. 대량의 용제를 사용하는 점이 문제로 지적되는 핵산의약품 생산에 있어 환경부하 저감 효과가 유럽을 비롯한 의약기업들에게 어필할 수 있을 것으로 기대하고 있다.
핵산의약품 CDMO 시장은 짧은 사슬 RNA 영역에 대한 신규진출이 잇따르고 있으며 긴 사슬 영역은 스미토모케미칼(Sumitomo Chemical) 등이 선도하고 있다.
아지노모토는 100-200 염기 핵산으로 유전자 치료에 대응하는 등 하이브리드 합성을 차별화 요소로 삼아 고상합성과 액상합성에 이어 제3의 기술로 육성할 계획이다.
또 GeneDesing에 따르면, 다수의 제약기업들이 화학수식한 300-400 염기 긴 사슬 RNA 양산이 가능해지면 신규 모달리티(치료법) 개발로 이어질 것으로 판단하고 거래를 문의하고 있는 것으로 알려졌다. (윤)





















 유전자 편집에 이용하는 가이드 RNA도 100-200개의 염기가 필요하며 화학수식한 염기를 도입하면 안정성과 활성 향상 개발이 가속화될 것으로 예상된다.
유전자 편집에 이용하는 가이드 RNA도 100-200개의 염기가 필요하며 화학수식한 염기를 도입하면 안정성과 활성 향상 개발이 가속화될 것으로 예상된다.
