세계적으로 코로나19(신종 코로나바이러스 감염증) 확산이 심각한 수준에 이르면서 치료제 및 백신 개발에 관심이 쏠리고 있다.
2020년 6월5일 기준 감염자가 발생한 지역 및 국가는 약 219개에 달하고 있으며 확진환자는 700만명, 사망자는 40만명에 육박한 것으로 파악되고 있다.
이에 따라 글로벌 제약기업을 중심으로 벤처기업 및 연구기관들이 치료제 및 백신 개발에 힘을 기울이고 있다.
치료제 없어 우선 기존 약물 활용
코로나19는 안전성, 유효성이 확립된 치료제가 없어 다른 치료제를 이용하는 방법이 우선시되고 있다.
미국 애브비(AbbVie)의 HIV(인체 면역결핍 바이러스) 감염증 치료제 칼레트라(Kaletra), 길리어드사이언스(Gilead Sciences)의 에볼라 치료제 렘데시비르(Remdesivir), 일본 후지필름도야마케미칼(Fujifilm Toyama Chemical)의 신종플루(신종 인플루엔자A) 치료제 아비간(Avigan) 등이 사용되고 있으며 임상시험 및 임상연구가 가속화되고 있다.
길리어드는 렘데시비르를 코로나19 환자에게 투약하는 대규모 임상시험을 시작했다.
일본에서는 테이진제약(Teijin Pharma)이 공급하고 있는 천식 치료제 알베스코(Alvesco)가 코로나19 치료에 효력을 발휘하는 것으로 확인됐으며, 중국에서는 추가이제약(Chugai Pharmaceutical)의 항체의약품 악템라(Actemra)가 과잉면역반응에 따른 염증이 발생한 중증환자에게 유효한 것으로 보고되고 있다.
악템라와 작용기전이 비슷한 의약품을 개발한 미국 리제네론(Regeneron)과 프랑스 사노피(Sanofi)는 유사약물을 이용한 임상시험을 진행하고 있다.
완치자 혈액 이용한 혈장치료 주목
최근에는 완치된 환자의 혈액을 이용하는 혈장치료가 주목받고 있다.
완치자 체내에서 생성된 신종 코로나바이러스에 대한 중화항체를 확진환자에게 투여하는 방법이며, 체내에서 성분을 채취함으로써 안전성이 보장되고 일반적인 신약 개발에 비해 빠른 실용화가 가능한 이점이 대두되고 있다.
미국 일라이릴리(Eli Lilly)는 캐나다 바이오기술 벤처기업과 제휴해 혈장치료법을 개발하고 있다. 이미 500개 이상의 항체 검출을 완료했으며 앞으로 4개월 이내에 임상시험을 시작할 계획이다.
리제네론도 수백개의 항체를 동정하고 있으며 유효한 항체 3개를 조합한 예방·치료제를 개발함에 따라 생산체제를 구축해 임상시험을 시작할 예정인 것으로 알려졌다.
사내 회의에서 100명 이상의 집단감염이 일어난 것으로 밝혀진 미국 바이오젠(Biogen)은 전 최고경영책임자(CEO)가 이끌고 있는 벤처기업 Vir Biotechnology와 제휴해 혈장치료법을 개발하고 있다.
일본에서는 다케다제약(Takeda Pharmaceutical)이 개발 계획을 공표했다.
2018년 인수한 샤이어(Shire)의 혈장분획제제 사업을 활용할 예정이며 미국을 중심으로 개발을 진행해 최단 9개월만에 실용화하겠다는 목표를 세우고 있다.
유전자치료제 개발기업 안제스(AnGes)는 오사카(Osaka)대학과 공동으로 개발하고 있는 DNA 백신을 적용한 혈장치료법을 개발하고 있으며 사람 대신 말에게 백신을 투여해 항체를 생산할 계획이다.
이밖에 도쿄(Tokyo)대학 연구그룹은 급성 췌장염 치료제 나파모스타트(Nafamostat)가 코로나19 치료에 효력을 발휘할 가능성을 발견하고 임상시험을 검토하고 있다.
국내에서는 바이오 의약품 메이저 셀트리온(Celltrion)이 항체치료제를 개발하고 있으며 의료기관으로부터 입수한 완치자 혈액으로 중화능력 검증을 실시해 최종 항체 후보군을 확정했다.
유전자 백신 개발에 기대감…
백신 개발 분야에서는 RNA, DNA 등 유전자 기술을 응용한 차세대제품에 대한 기대가 높아지고 있다.
미국 모더나(Moderna)가 세계 최초로 사람에 대한 임상시험을 시작한 백신은 인체 감염의 발판이 되는 단백질을 코딩한 mRNA(messenger RNA)를 이용한 백신으로 바이러스 없이 인공적으로 합성할 수 있어 안전하게 단기간 개발이 가능한 것으로 파악되고 있다.
기존에 채용되고 있는 달걀배양법은 바이러스 분리부터 백신 공급까지 5-8개월이 소요되나 DNA 백신은 약 2개월만에 실용화할 수 있는 것으로 알려졌다.
벤처기업들도 백신 임상시험에 박차를 가하고 있다.
미국 이노비오(,Inovio Pharmaceuticals)는 미국, 한국, 중국에서 DNA 백신 임상시험을, 독일 바이온텍(BioNTech)은 화이자(Pfizer) 및 중국기업과 제휴해 미국, 유럽, 중국에서 mRNA 백신 임상시험을 시작할 방침이다.
안제스는 DNA 백신 임상시험을 계획하고 있으며 미츠비시타나베제약(Mitsubishi Tanabe Pharma)의 캐나다 자회사 메디카고(Medicago)는 식물 베이스 백신을 개발해 현지에서 임상시험을 진행할 예정이다.
글로벌 제약 메이저들은 정부기관에 협력해 백신 개발을 지원하고 있다.
존슨앤존슨(Johnson & Johnson)은 미국 보건복지부 산하 생물의약품첨단연구개발국(BARDA)과 제휴해 백신 후보를 연구하고 있으며 자회사인 얀센(Janssen)의 화합물 라이브러리를 활용한 치료제 탐색에도 협력하고 있다.
영국 GSK(GlaxoSmithKline)는 국제민간기구인 전염병 혁신 연합(CEPI)을 통해 백신 효과를 향상시키는 보조제 기술을 제공하고 있다.
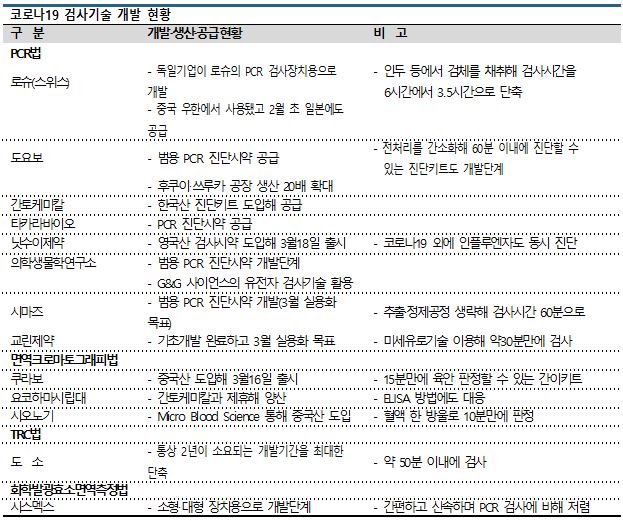
PCR 이어 진단키트 개발 잇달아…
코로나19 감염이 빠르게 확산됨에 따라 진단시약에 대한 관심이 높아지고 있다.
최근에는 국내에서 제안한 PCR(유전자 증폭) 검사기법이 국제표준화를 앞두고 있으며 새로운 진단키트 개발 움직임도 잇따르고 있다.
온도를 조절해 유전자 증폭을 반복하는 PCR 검사는 구인두, 비인두에서 유전자를 추출해 정제하는 작업이 복잡할 뿐만 아니라 결과가 나오기까지 6시간 이상이 소요됨에 따라 검사시간 단축이 요구되고 있다.
스위스 로슈(Roche)는 약 3.5시간만에 검사할 수 있는 PCR 진단시약을 공급하고 있으며 일본도 2020년 2월 초 민간검사기관에 검사를 위탁하는 과정에서 해당제품을 코로나19 검사지침에 추가했다.
일본에서는 도요보(Toyobo) 등이 PCR 진단시약을 공급하고 있으며 신기술 개발이 잇따르고 있다.
교린제약(Kyorin Pharmaceutical)은 검사시간을 약 30분으로 단축하는 기술을 개발해 실용화를 추진하고 있으며 인플루엔자 등 다른 호흡기 감염증과 신속하게 판별하는데 기여할 수 있을 것으로 기대하고 있다.
닛수이제약(Nissui Pharmaceutical)은 영국기업의 다항목 검사 시스템을 도입해 2020년 3월18일 출시했다. 항원항체반응을 이용하는 면역크로마토그래피법은 인플루엔자 진단키트와 같이 단시간에 간편하게 진단할 수 있는 특징이 있다.
일본 쿠라보(Kurabo)는 중국 제휴기업이 개발한 진단키트를 도입해 3월16일부터 공급을 시작했다. PCR 기법으로 검출하기 어려운 감염 초기단계도 판정할 수 있어 위음성이 거의 나오지 않는 것으로 파악되고 있다.
독자기술을 활용한 연구개발(R&D)도 가속화되고 있다.
에이켄케미칼(Eiken Chemical)은 목적 유전자를 무한하게 증폭시킬 수 있는 LAMP법을 개발했고, 바이러스 유무를 매우 정밀하게 검출할 수 있는 강점이 주목받고 있다.
도소(Tosoh)는 RNA를 직접 증폭시킬 수 있는 TRC법이 RNA 바이러스인 신종 코로나바이러스 검출에 적합할 것으로 판단하고 개발에 착수했다.